副反応疑い報告制度
更新日:2026年3月31日
ページ番号:40994700
予防接種法に基づく副反応疑い報告制度の概要
ワクチン接種の副反応とは
ワクチンの接種により、副反応(副作用)が起きることがあります。
多くは、発熱したり、注射した部分が腫れるといった、比較的軽く、短期間で治るものですが、ごくまれに、重いアレルギーなど、重症の副反応が起きることがあります。
副反応疑い報告
副反応疑い報告とは、予防接種法第12条第1項の規定に基づき、医師等が、定期の予防接種又は臨時の予防接種(定期の予防接種等)を受けた者が一定の症状を呈していることを知った場合に、厚生労働省に報告しなければならない制度です。
報告には偶発的なものや他の原因によるものなど、ワクチン接種との関連がないものも含まれます。
この制度は、予防接種後に生じる種々の身体的反応や副反応について情報を収集し、ワクチンの安全性について管理・検討を行い、広く国民に情報を提供すること及び今後の予防接種行政の推進に資することを目的としています。
厚生科学審議会(副反応検討部会)
収集した報告については、厚生労働省の審議会に報告され、定期接種として広く皆さまに接種していただく上で安全性に問題が無いか、専門家による評価が行われます。
報告の流れ
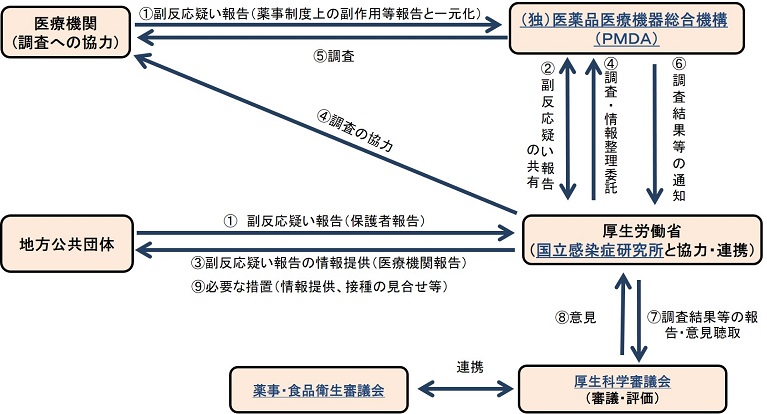
関連サイト
予防接種法に基づく医師等の報告のお願い(厚生労働省)(外部サイト)![]()
厚生科学審議会 (予防接種・ワクチン分科会 副反応検討部会)(厚生労働省)(外部サイト)![]()
副反応疑い報告制度と予防接種健康被害救済制度の違い
接種後に起きた症状とワクチンとの因果関係の考え方について、副反応疑い報告制度では医学・薬学的観点から総合的に判断する一方で、健康被害救済制度では厳密な医学的な因果関係を必要としない等、考え方に違いがあります。
そのため前者の制度で評価できないとされた事例でも、後者の制度で認定される場合があります。
副反応疑い報告制度
原疾患との関係、薬理学的な観点や時間的な経過などの要素を勘案し、医学・薬学的観点から総合的に判断し、ワクチン接種と副反応疑い事象の因果関係の評価が行われています。
個別症例の評価や集団での系統的な分析・評価により安全性等を評価した上で、必要な措置が講じられます。
健康被害救済制度
接種に係る過失の有無にかかわらず、厚生労働省の審査会において予防接種と健康被害との因果関係が認定された方を、迅速に救済するものです。
その認定にあたっては、請求された疾病等と予防接種との因果関係について、厳密な医学的な因果関係までは必要とせず、接種後の症状が予防接種によって起こることを否定できない場合も対象とするとの考え方に基づいて審査が行われます。
個々の事例における因果関係の判断にあたって、副反応疑い報告制度における評価は勘案していないため、仮に副反応疑い報告制度において因果関係が評価できないとされている事例であっても、健康被害救済の対象となる場合があります。
関連サイト
接種後に起きた症状とワクチンとの因果関係の考え方について、副反応疑い報告制度と健康被害救済制度では、どうなっていますか。(厚生労働省)(外部サイト)![]()
予防接種健康被害救済制度について(厚生労働省)(外部サイト)![]()
被接種者または保護者による副反応疑い報告
医師だけでなく、被接種者本人または保護者の方も、定期の予防接種後に発症した健康被害について、必要に応じて市町村に報告することができます。
市町村へ報告された健康被害は、「予防接種後に発生した症状に関する報告書(保護者報告用)」を用いて、都道府県を通じて厚生労働省へ報告されます。
詳しくは、健康増進課までお問い合わせください。
![]() 予防接種後に発生した症状に関する報告書 (保護者報告用)(PDF:107KB)
予防接種後に発生した症状に関する報告書 (保護者報告用)(PDF:107KB)
(参考)独立行政法人医薬品医療機器総合機構(PMDA)への報告
独立行政法人医薬品医療機器総合機構(PMDA)では、医薬品の安全対策に活用する目的で、患者の皆様またはご家族から、医薬品による副作用報告を受付、整理し、厚生労働省へ報告しています。
詳しくは以下のリンク先をご確認ください。
患者副作用報告の取組の概要(独立行政法人医薬品医療機器総合機構(PMDA))(外部サイト)![]()
患者の皆様からの医薬品副作用報告(独立行政法人医薬品医療機器総合機構(PMDA))(外部サイト)![]()
定期予防接種及び臨時接種の副反応疑い報告件数(西宮市)
西宮市に情報提供がありました定期予防接種及び臨時接種の副反応疑い報告件数は以下のとおりです。(令和8年3月31日時点)
| 年度 | 報告件数 | 左記のうち 症状が「重い」※ | 内訳 |
|---|---|---|---|
| 令和7年度 | 3 | 2 | 小児用肺炎球菌(1件、うち重い0件) ロタ(1件、うち重い1件) 帯状疱疹(1件、うち重い1件) |
| 令和6年度 | 5 | 1 | HPV(2件、うち重い1件) BCG(3件、うち重い0件) |
| 令和5年度 | 4 | 2 | ヒブ・小児用肺炎球菌・B型肝炎・四種混合・ロタ(1件、うち重い1件) ヒブ・小児用肺炎球菌・B型肝炎・四種混合(1件、うち重い0件) HPV(2件、うち重い1件) |
| 令和4年度 | 0 | 0 | ー |
| 令和3年度 | 0 | 0 | ー |
| 年度 | 報告件数 | 左記のうち 症状が「重い」※ |
|---|---|---|
令和7年度 | 5 | 2 |
| 令和6年度 | 8 | 7 |
| 令和5年度 | 9 | 5 |
令和4年度 | 36 | 23 |
| 令和3年度 | 146 | 29 |
※報告件数のうち、症状が「重い」と報告された件数です。
「重い」とは、症状の程度が以下の1~7のいずれかに該当すると医師が判断したものです。
1 死亡 2 障害 3 死亡につながるおそれ 4 障害につながるおそれ
5 入院 6 1~5に準じて重い 7 後世代における先天性の疾病又は異常
医療機関の皆様へ
予防接種法に基づき、医療機関の開設者又は医師が、定期の予防接種等を受けた方が、それが原因によるものと疑われる症状を呈していると知ったときは、報告(副反応疑い報告)をお願いします。
報告をいただくことで、予防接種後に生じる種々の身体的反応や副反応疑いについて情報を収集することができ、ワクチンの安全性の評価・管理や、医療従事者・国民の皆様への情報提供に役立てられます。
また、収集された報告については、厚生労働省の審議会に報告され、専門家による評価が行われます。
こうした結果を公表するなどして、安全性に関する情報提供などが行われます。
報告対象
医療機関の開設者又は医師が、予防接種法施行規則第5条に規定する症状を診断した場合
注意事項
- 定期の予防接種以外の予防接種(任意の予防接種)による健康被害についても、医薬品医療機器等法に基づき、薬局開設者、病院若しくは診療所の開設者又は医師、歯科医師、薬剤師その他医薬関係者が、保健衛生上の危害の発生又は拡大を防止する観点から報告の必要があると認める場合は、同様に報告しなければなりません。
- 副反応疑い報告は、発生した症状と予防接種との因果関係が必ずしも明らかでない場合であっても、保健衛生上の危害の発生又は拡大を防止する観点から報告の必要があると判断される場合には、報告対象となり得ます。
- 報告基準として設定した症状については、ワクチンとの関連によらず、接種後の発生までの時間以内に発生した場合が報告の対象です。
- 例えば、アナフィラキシーについては、ワクチンとの関連によらず、接種後4時間以内に発生した場合が報告の対象です。
- 副反応疑い報告は医薬品医療機器等法に基づく報告としても取り扱うこととしております。
そのため、医療機関から重ねて医薬品医療機器等法に基づく報告を行う必要はありません。
報告様式
予防接種後副反応疑い報告について「電子報告システム」からご提出ください。
(記載誤り等防止の観点からも電子報告をご利用ください。)
電子報告が困難な場合は、予防接種後副反応報告書をFAXにて送付することもできます。
詳しくは以下のリンク先「予防接種法に基づく医師等の報告のお願い」をご確認ください。
予防接種法に基づく医師等の報告のお願い(厚生労働省)(外部サイト)![]()
PDF形式のファイルを開くには、Adobe Acrobat Readerが必要です。
お持ちでない方は、Adobe社から無償でダウンロードできます。
![]()
